O parecer do técnicos da Anvisa destacou falta de documentos e possíveis riscos à saúde em resposta a pedido de importação
Anvisa reprova importação e aplicação da vacina Sputnik V no Ceará e em outros estados brasileiros
Em reunião extraordinária realizada na noite desta segunda-feira (26), a Agência Nacional de Vigilância Sanitária) decidiu reprovar a compra e aplicação “excepcional e temporária” da Sputnik V no Brasil. O pedido de importação da vacina russa foi feito por 14 governos estaduais, inclusive o Ceará.
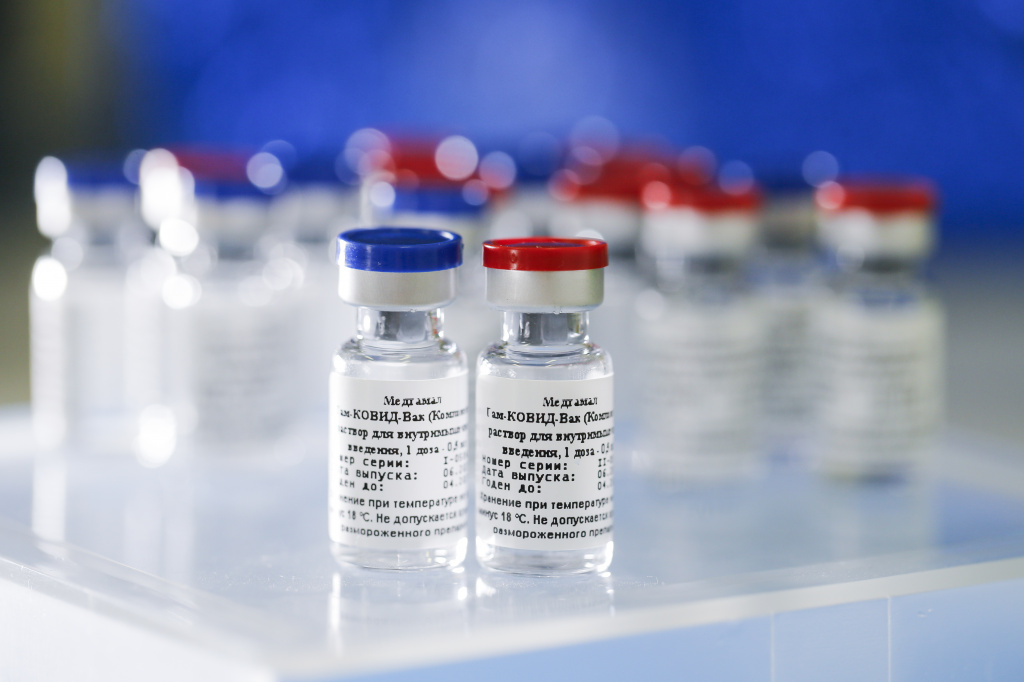
No último dia 12, o governador Camilo Santana havia entrado com uma ação no Supremo Tribunal Federal (STF) para que a Anvisa autorizasse a utilização de 5,87 milhões do imunizante junto ao Fundo Soberano Russo.
Durante a reunião, o gerente geral de Medicamentos e Produtos Biológicos da Anvisa, Gustavo Mendes, argumentou que o fabricante da Sputnik V não apresentou a análise de segurança da vacina por faixa etária, por comorbidades e para soropositivos para o SARS-CoV-2. Além disso, a empresa também não demonstrou que controla de forma eficiente o processo para evitar outros vírus contaminantes durante a produção do imunizante.
Leia também | Vacinação em Fortaleza: confira a lista de agendamento desta terça-feira (27)
Em relação à tecnologia usada na produção da vacina, a de adenovírus replicante, o especialista afirmou que as células onde os adenovírus são produzidos permitem que sua capacidade de replicação seja readquirida.
>>Siga o GCMAIS no Google Notícias<<<
“A presença de adenovírus replicante pode ter impactos na segurança da vacina, porque o vírus que não deveria ser replicante […] quando se replica pode causar adenovirose e se acumular em tecidos específicos do corpo […] A Gerência Geral de Medicamentos e Produtos Biológicos não recomenda a importação da Sputnik V”, comentou Mendes.
Outros dois técnicos também deram parecer contra a Sputinik V: Ana Carolina Marino, gerente-geral de Fiscalização, e Suzie Marie Gomes, Gerente Geral de Monitoramento.
>>Acompanhe a TV Cidade Fortaleza no YouTube<<<
Para tomar a decisão, a Anvisa inspecionou este mês duas fábricas da Sputnik na Rússia para levantar dados que faltavam sobre a produção da vacina e que não haviam sido apresentados pela União Química, farmacêutica que representa o imunizante no Brasil, no pedido de uso emergencial enviado no dia 26 de março.
Em uma das fábricas a agência observou não conformidades que impactaram na garantia de esterilidade do imunizante. Além disso, também foram identificadas falhas no desenvolvimento da vacina, nos estudos conduzidos e na qualidade do produto finalizado.
Na visita, de acordo com a gerente de inspeção, Ana Carolina Merino, foram constadas não conformidades na fabricação da vacina, que impactam, entre outras, na garantia de esterilidade do produto. “Neste momento, o risco inerente à fabricação não é possível de ser superado, tanto para o insumo fabricado pela Generium quanto pelos produtos acabados fabricados pela Generium e pela UfaVITA, então a nossa gerência não recomenda a importação da vacina”, afirmou.
Em outro parecer, a gerente-geral de Monitoramento de Produtos Sujeitos à Vigilância Sanitária da Anvisa, Suzie Marie Gomes, afirmou haver falta de informações conclusivas sobre eventos adversos de curto, médio e longo prazos decorrentes do uso da vacina, o que prejudica a avaliação do produto. “Eu chamo a atenção também para que a ausência de dados também é informação. A ausência de comprovação é considerada uma evidência, e uma evidência forte, sobretudo quando temos uma estimativa de população exposta ao risco que beira os 15 milhões de cidadãos”, afirmou.
Por fim, a Anvisa ressaltou ainda que não teve autorização para entrar no Instituto Gamaleya, o desenvolvedor da vacina Sputinik V.
Com informações do R7 e Agência Brasil

NOTÍCIAS DO GCMAIS NO SEU WHATSAPP!
Últimas notícias de Fortaleza, Ceará e Brasil
Lembre-se: as regras de privacidade dos grupos são definidas pelo Whatsapp.
RELACIONADAS

WhatsApp lança recurso de transcrição de áudios em vários idiomas

Menina de seis anos é sequestrada no Crato; motorista suspeito é preso

José Sarto anuncia força-tarefa para garantir medicamentos e insumos para o IJF
